pH(ペーハー)とは、溶液の「酸性、アルカリ性の程度」を表す指標です。pH の意味と、pH を計算するために重要な4つのポイントを解説します。
pH とは
$\mathrm{pH}=-\log_{10}[\mathrm{H}^+]$
ただし、$[\mathrm{H}^+]$ とは、水素イオンのモル濃度($\mathrm{mol/L}$)です。
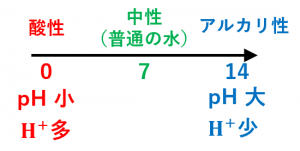
pH が小さいほど強い酸性です。
pH が普通(6~8くらい)の場合は中性です。
pH が大きいほど強いアルカリ性です。
このように、pH は酸性、アルカリ性の程度を表します。
pH の計算の基本
水素イオン濃度を求めれば pH が計算できます。
例題:
$0.1\:\mathrm{mol/L}$ の塩酸の pH を計算してみましょう。
解答:
塩酸の化学式は $\mathrm{HCl}$ です。つまり、1つの $\mathrm{HCl}$ に対して1つの $\mathrm{H}^+$ が対応します(塩酸は1価の強酸です)。よって、$0.1\:\mathrm{mol/L}$ の塩酸の水素イオン濃度は $0.1\:\mathrm{mol/L}$ です。
よって、pH は、
$\mathrm{pH}=-\log_{10}[\mathrm{H}^+]\\
=-\log_{10}0.1\\
=-\log_{10}10^{-1}\\
=1$
となります。
価数に注意する
水素イオン濃度を計算する際には価数(いくつの $\mathrm{H}^+$ が対応するか?)に注意しましょう。
例題:
$0.01\:\mathrm{mol/L}$ の硫酸の pH を計算してみましょう。ただし、$\log_{10}2=0.3$ とします。
解答:
硫酸の化学式は $\mathrm{H_2SO_4}$ です。つまり、1つの $\mathrm{H_2SO_4}$ に対して2つの $\mathrm{H}^+$ が対応します(硫酸は2価の強酸です)。よって、$0.01\:\mathrm{mol/L}$ の硫酸の水素イオン濃度は $0.02\:\mathrm{mol/L}$ です。
よって、pH は、
$\mathrm{pH}=-\log_{10}[\mathrm{H}^+]\\
=-\log_{10}0.02\\
=-\log_{10}(2\times 10^{-2})\\
=2-\log_{10}2\\
=1.7$
となります。
電離度を考慮する
水素イオン濃度を計算する際には電離度(何割が $\mathrm{H}^+$ を生成するか?)に注意しましょう。
例題:
$0.001\:\mathrm{mol/L}$ の酢酸の pH を計算してみましょう。ただし、酢酸の電離度を $0.01$ とします。
解答:
酢酸の化学式は $\mathrm{CH_3COOH}$ です。つまり、1つの $\mathrm{CH_3COOH}$ に対して1つの $\mathrm{H}^+$ が対応します。ただし、電離度が $0.01$ なので、全体のうち $0.01$ の割合だけが電離して水素イオンを発生させます。
よって、pH は、
$\mathrm{pH}=-\log_{10}[\mathrm{H}^+]\\
=-\log_{10}(0.001\times 0.01)\\
=-\log_{10} 10^{-5}\\
=5$
となります。
ここまでの3つのポイントをまとめると、酸性溶液の pH は、
$-\log_{10}(モル濃度 × 価数 × 電離度)$
で計算できることが分かります。
塩基の pH を計算する
アルカリ性溶液の pH は、
$\mathrm{pH}=14+\log_{10}[\mathrm{OH}^-]$
という公式で計算します。
例題:
$0.01\:\mathrm{mol/L}$ の水酸化ナトリウムの pH を計算してみましょう。
解答:
水酸化ナトリウムの化学式は $\mathrm{NaOH}$ です。つまり、1つの $\mathrm{NaOH}$ に対して1つの $\mathrm{OH}^-$ が対応します(水酸化ナトリウムは1価の強塩基)。
よって、pH は、
$\mathrm{pH}=14+\log_{10}[\mathrm{OH}^-]\\
=14+\log_{10}(0.01)\\
=14+\log_{10} 10^{-2}\\
=12$
となります。
次回は テスラ(T)⇔ガウス(G)の変換方法と、磁場の強さのイメージ を解説します。